Antigen-Schnelltests liefern schnell ein Ergebnis über eine Corona-Infektion – die Genauigkeit lässt, anders als beim PCR-Test, jedoch zu wünschen übrig. Ein Verbund der Fraunhofer-Institute für Produktionstechnologie IPT, für Grenzflächen- und Bioverfahrenstechnik IGB sowie des Fraunhofer Center for Manufacturing Innovation CMI in Boston (USA) forscht daher an einer zugleich schnellen und genauen Alternative. Der Pathogen Analyzer nutzt den LAMP-Test in einem patentierten, druckbaren Hydrogel und ist schnell auf weitere Pathogene übertragbar.
OmniTest – Nanogel-Biosensoren für schnelle und sichere Pathogendiagnostik
Wer kennt es nicht? Der Hals kratzt, Schlappheitsgefühl macht sich breit. Hat man sich mit Corona infiziert? Über Antigen-Schnelltests kann man dies zuhause schnell überprüfen – die Genauigkeit dieser Tests lässt jedoch zu wünschen übrig. Viele Infektionen bleiben unerkannt, auch kann es zu fehlerhaften Positiv-Ergebnissen kommen. Für einen sicheren Nachweis ist ein PCR-Test unerlässlich, allerdings ist dieser sowohl deutlich teurer als auch langwieriger.
Schnelle und sichere Ergebnisse
Ein Verbund aus Forscherinnen und Forschern des Fraunhofer-Instituts für Produktionstechnologie IPT, des Fraunhofer-Instituts für Grenzflächen- und Bioverfahrenstechnik IGB sowie des Fraunhofer Center for Manufacturing Innovation CMI in Boston (USA) möchte das nun ändern. Die drei Institute entwickeln zusammen den Pathogen Analyzer SECURIGEL (Abb. 1) und verbinden damit die Vorteile von Antigen- und PCR-Tests: Schnelligkeit und Genauigkeit.
Amplifikation bei konstanter Temperatur
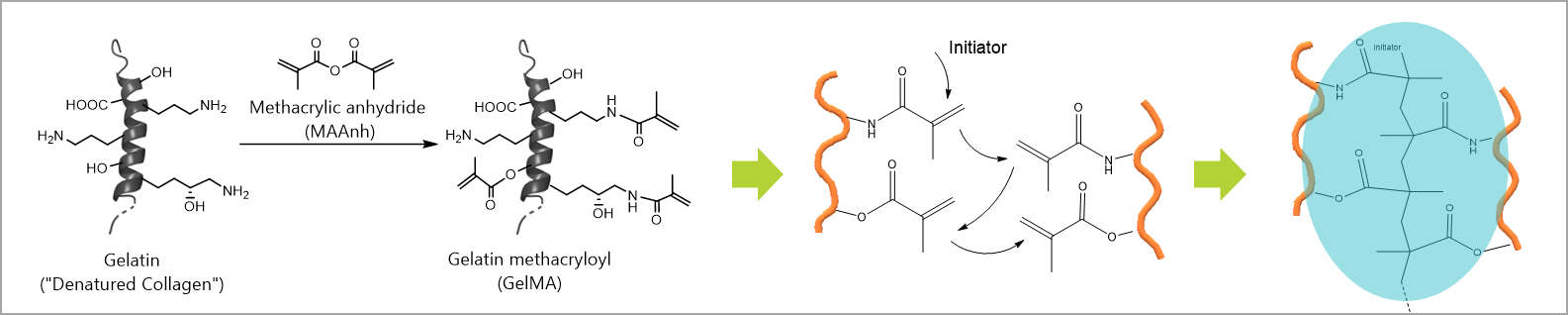
Um das Erbgut zu vervielfältigen, nutzen die Institute ein anderes Verfahren als beim PCR-Test. So liegt das Ergebnis nun bereits nach ca. 30 Minuten vor. Das Herzstück der Technologie ist die Verkapselung und On-Chip-Speicherung einer erregerspezifischen Diagnostik mittels RT-LAMP (reverse transcription loop-mediated isothermal amplification) in einem patentierten, druckbaren Hydrogel (Abb. 2). Die Reaktion zur Amplifikation der Virus-RNA findet bei einer konstanten Temperatur von 62 °C statt – das in der PCR nötige Aufheizen und Abkühlen der Probenflüssigkeit entfällt.
Multiplexing durch Hydrogel
Dazu haben wir am Fraunhofer IGB und am Fraunhofer CMI auf einem Testchip, der ähnlich groß ist wie ein Antigen-Schnelltest, zahlreiche kleine Hydrogel-Tropfen aufgedruckt (Abb. 3). Diese Biogel-Nanosensoren sind in 1500 einzelnen 500 pL-Spots angeordnet, mit jeweils 500 zusätzlichen Spots für gleichzeitige Positiv- und Negativkontrollen, was die Genauigkeit und Zuverlässigkeit der Ergebnisse erhöht. Das Hydrogel wurde am Fraunhofer IGB für die Haftung der Tropfen auf der Chipoberfläche und die Reaktion für ein korrektes Testergebnis optimiert. Unser Hydrogel (Abb. 2 und 4) zeichnet sich demnach durch fünf Merkmale aus: Möglichkeit zum räumlichen Multiplexing, niedrigere Nachweisgrenzen, On-Chip-Speicherung der Reagenzien, längere Haltbarkeit und Skalierbarkeit. Der entscheidende Vorteil unseres Ansatzes ist eine vereinfachte Probenvorbereitung und Diskretisierung – also die Gewinnung von endlich vielen (»diskreten«) Daten aus einem kontinuierlichen Informationsfluss − von RT-LAMP, um falsch-positive Ergebnisse deutlich zu reduzieren.
Paralleler Nachweis mehrerer Pathogene
Ein solcher Multiplexing-Ansatz erhöht zum einen die Verlässlichkeit, zum anderen ermöglicht er es, bis zu zwölf verschiedene Virenarten gleichzeitig mit einer Probennahme und einem Chip nachzuweisen. Da wir das System als Baukastensystem entwickelt haben, lässt es sich schnell an neue Pathogene und damit neue Situationen anpassen.
Angebot und Zusammenarbeit

Vorteile und Technologiereife
Unsere Lösung zeichnet sich durch verschiedene Vorteile gegenüber den derzeitig verfügbaren Produkten aus:
- Schnelles und zugleich genaues Ergebnis
- Keine Probenpräparation erforderlich, wodurch Tests auch zu Hause durchgeführt werden könnten
- Druckprozess ermöglicht räumliches Multiplexing, sodass mit einer Untersuchung auf viele unterschiedliche Erreger getestet werden kann
Die Machbarkeit mit unserem Lösungsansatz wurde erfolgreich gezeigt (TRL 3-4). Nun steht die Optimierung des Sensor-Layouts und die Übertragung auf kostengünstige, skalierbare Produktionsverfahren an.
Zusammenarbeit
Da wir das System als Baukastensystem entwickelt haben, lässt es sich schnell an kundenspezifische Fragestellungen wie neue Pathogene anpassen. Bei Interesse an der gemeinsamen Weiterentwicklung zu einem marktreifen Produkt kommen Sie gerne auf uns zu.
Anwendungsbereiche sehen wir überall dort, wo schnell eine Information erforderlich ist, ob und mit welchen Pathogenen eine Person infiziert ist. Dies kann beispielsweise zur Eingangskontrolle in Bereichen mit erhöhter Ansteckungsgefahr (Krankenhäuser, Pflegeeinrichtungen) der Fall sein. Durch Anpassung des Erregerspektrums auf dem Sensor eignet dieser sich auch zur Überwachung von Mikroorganismen in der Umwelt, in der Lebensmittelproduktion oder zur Qualitätskontrolle in der Pharmaproduktion.
Eine Hauptfunktion unseres patentiertes Hydrogels liegt in der Stabilisierung von Biomolekülen (Proteine, Enzyme). Das Hydrogel bietet daher auch für die Entwicklung weiterer Produkte, z. B. anderer Test-Assays, Formulierungen oder Oberflächenmodifizierungen, große Vorteile.
Projektinformationen
Projekttitel
OmniTest – Nanogel-Biosensoren für schnelle und sichere Pathogendiagnostik
Projektlaufzeit
Juni 2021 – Dezember 2022
Projektpartner
- Fraunhofer Center for Manufacturing Innovation CMI, Boston (USA)
- Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
- Fraunhofer-Institut für Produktionstechnologie IPT
Projektkoordination
- Fraunhofer Center for Manufacturing Innovation CMI, Boston (USA), Dr. Christine McBeth
Förderung
Fraunhofer (Ausschreibung/Programm: PACT)
 Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB

