
3D-In-vitro-Modell zur Validierung von Immunrezeptoren als Targets für die Behandlung von Psoriasis
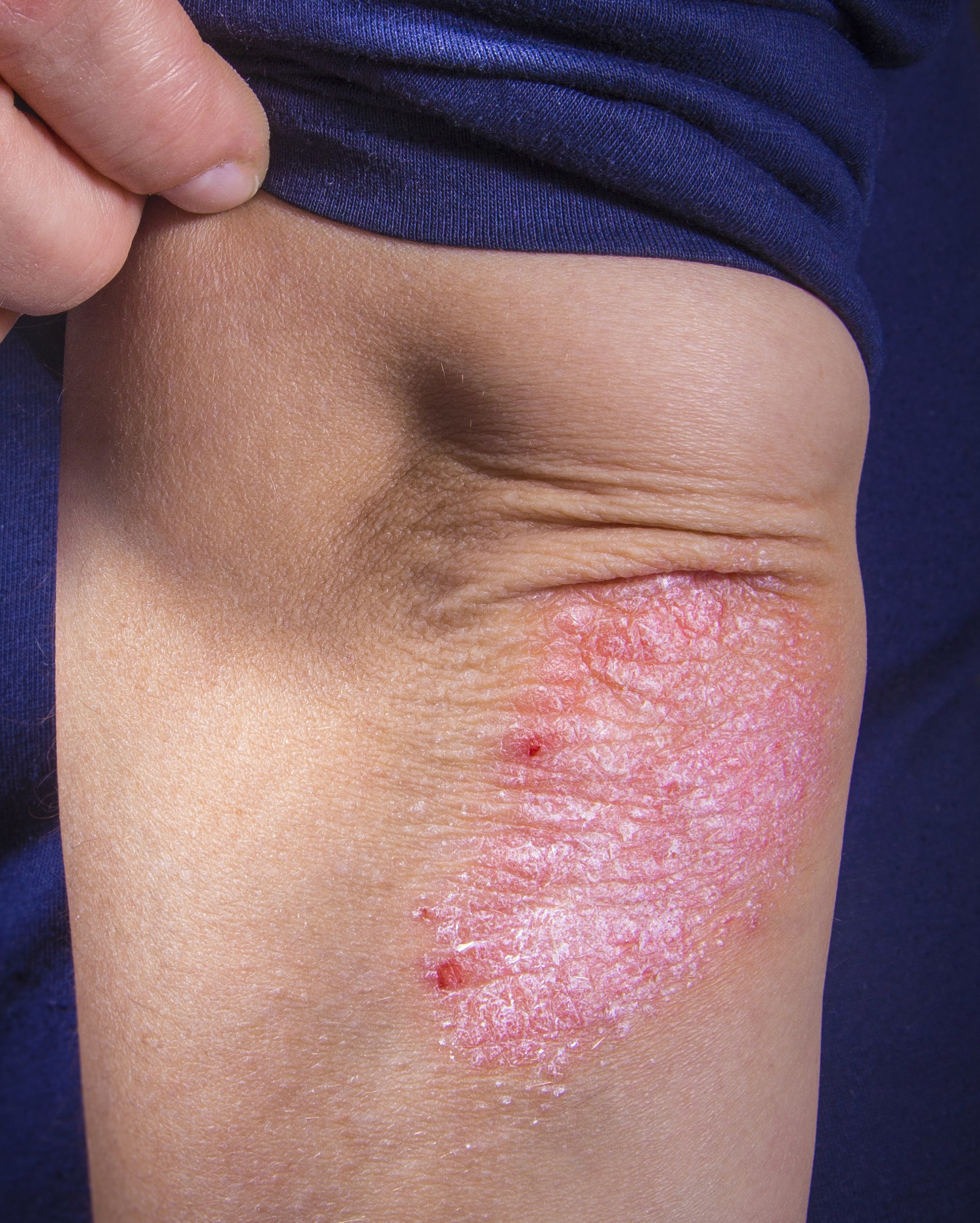
Psoriasis (Schuppenflechte) ist eine chronische Autoimmunkrankheit, von der etwa zwei Prozent der Bevölkerung weltweit betroffen sind [1]. Die Krankheit äußert sich in Form von entzündeten und schuppenden Hautstellen, die mit Juckreiz und Schmerzen einhergehen. Zu den derzeitigen Psoriasis‑Behandlungen gehören systemisch wirkende Biologika wie monoklonale Antikörper sowie topisch angewandte hydrokortisonhaltige Salben. Oftmals sind die Therapieoptionen mit zum Teil schweren Nebenwirkungen verbunden oder die Patienten sprechen darauf nicht an.
Um molekulare Angriffspunkte für eine gezielte immunmodulatorische Behandlung zu identifizieren, werden humane In‑vitro‑Modelle benötigt, die die pathologisch veränderte humane Psoriasish-Haut darstellen. Diese Modelle müssen valide und reproduzierbar und damit für größere Testreihen geeignet sein. In der Forschung werden vor allem Mausmodelle eingesetzt, deren Aussagekraft aufgrund der geringen Übertragbarkeit auf den Menschen stark begrenzt ist. Alternativ werden Modelle basierend auf Patientenbiopsien eingesetzt, die sich durch eine limitierte Verfügbarkeit des Ausgangsmaterials nicht für ein Wirkstoffscreening eignen.
Neues 3D‑Psoriasis-Epidermismodell
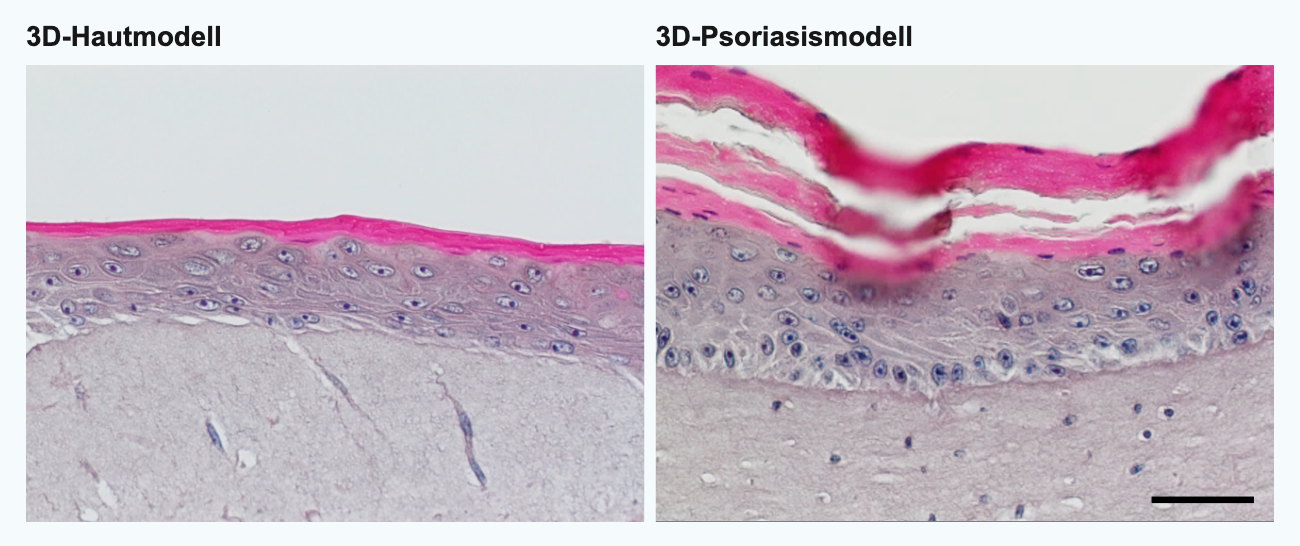
Im Innovationsfeld Zell- und Gewebetechnologien des Fraunhofer IGB wurde erfolgreich ein ganz neuartiges 3D‑Psoriasis‑Hautmodell etabliert, welches diese Probleme umgeht. Die Grundlage für das Modell sind humane immortalisierte Keratinozyten, die in vitro zu einer mehrlagigen Epidermis ausdifferenziert werden. Durch Überexpression des Psoriasis-assoziierten Transkriptionsfaktors STAT3 in diesen Keratinozyten, die Kokultivierung des Epidermismodells mit in vitro aktivierten T‑Zellen und die gezielte Zugabe von proinflammatorischen Zytokinen ist es uns gelungen, die Psoriasis‑typische Entzündungsreaktion in den Modellen nachzustellen. Ein Vergleich mit Patientenbiopsien bestätigte die Übereinstimmung der Psoriasismarker im In‑vitro‑Modell.
Validierung von Toll-like-Rezeptoren als Targets für Psoriasis-Therapeutika
Dieses Modell wurde bereits erfolgreich für die Validierung von Rezeptoren des angeborenen Immunsystems, sogenannten Toll‑like‑Rezeptoren (TLR), als Targets eingesetzt. Hierfür haben wir TLR‑Agonisten – Moleküle, die TLR aktivieren – mit dem neuen Psoriasis-Modell getestet und nach Zugabe dieser Agonisten die Expression von spezifischen Psoriasismarkern nachgewiesen. Mit einem Psoriasis-Modell, bei welchem TLR2 in den Keratinozyten durch ein Knock‑out ausgeschaltet wurde, konnten wir zeigen, dass die Expression von Psoriasismarkern nach Zugabe von TLR2‑Agonisten signifikant reduziert wurde.
Ausblick
Auf Basis des neuen am IGB etablierten humanen 3D‑In‑vitro‑Psoriasis-Modells konnten Toll‑like‑Rezeptoren erstmals als Target für die Behandlung von Psoriasis validiert werden. In einem nächsten Schritt wollen wir Moleküle mit TLR inhibierender Wirkung als potenzielle Wirkstoffe evaluieren.
Das humane 3D‑In‑vitro‑Psoriasis-Modell eignet sich auch optimal für die Testung neuer immunmodulatorischer Moleküle. Zudem bietet es den Vorteil, dass es auch für andere entzündliche Hauterkrankungen wie die atopische Dermatitis angepasst werden kann.
 Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB